Учёные обнаружили новую комбинацию веществ, убивающую раковые клетки
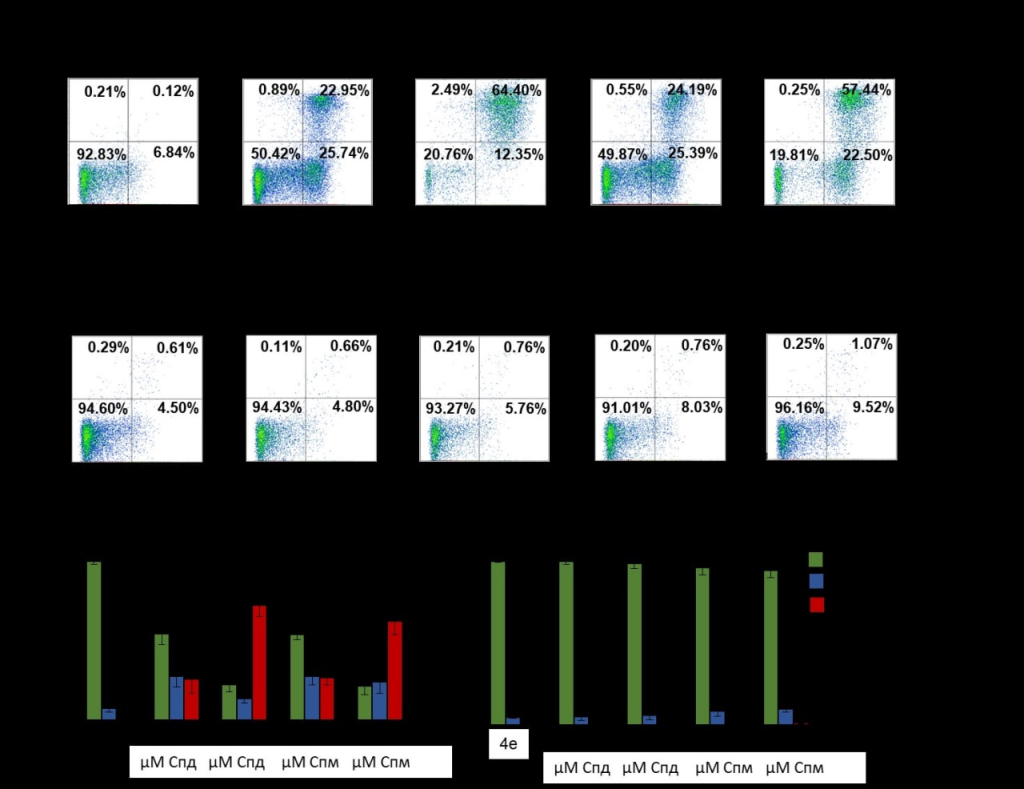
Индукция апоптоза в опухолевых клетках с помощью биспидинового соединения в присутствии полиаминов. Клетки (А) модели опухоли печени человека HepG2 или (Б) нормальные фибробласты линии WI-38 инкубировали с соединением 4e и полиаминами 1 или 10 мкм спермидина (Спд) или спермина (Спм). Представлены результаты проточной цитометрии. Увеличение количества клеток в верхних частях диаграмм соответствует увеличение гибели клеток.
Учёные нашли новую комбинацию полиаминов с биспидиновым производным, которые вместе способны избирательно убивать раковые клетки. В частности, в опухолевых клетках запускается программа контролируемой гибели, известная как апоптоз. Работу провела группа исследователей во главе со специалистами Института биомедицинской химии имени В.Н. Ореховича (ИМБХ) и Российского университета дружбы народов.
Они выяснили, что каждый из компонентов в отдельности не оказывает смертоносного действия на раковые клетки — оно проявляется только в составе комбинации. В ее состав входят природные полиамины и производное биспидина. Природные полиамины — это небольшие линейные молекулы с 3 или 4 положительными зарядами вдоль своей длины. Второй компонент, производное биспидина, также содержит фиксированный положительный заряд на одном из своих боковых «хвостов».
Первоначальной целью исследования был поиск активаторов распада полиаминов в клетке. Дело в том, что полиамины подобны обоюдоострому мечу. С одной стороны, они жизненно необходимы каждой клетке для нормальной жизнедеятельности, особенно опухолевым клеткам для их постоянного и неконтролируемого роста. С другой стороны, продукты окисления или расщепления полиаминов как раз и запускают тот самый апоптоз.
Характерная полиаминам двойственность действия в зависимости от их концентраций и от присутствия окисляющих ферментов давно привлекает внимание учёных. Этот метаболический путь активно изучается как потенциальная терапевтическая мишень при опухолевых процессах. Казалось бы, достаточно снизить концентрацию полиаминов в клетке, и она снова превратится из опухолевой в нормальную. Блокировка их синтеза, однако, не приводит к ожидаемому противропухолевому эффекту, так как влечет компенсаторное поглощение опухолью этих молекул из окружающей среды. Альтернативный подход — активация распада полиаминов, сопряженного с образованием токсических продуктов — выглядит перспективным, и именно он был апробирован научным коллективом ИМБХ и РУДН.
Сначала учёные протестировали набор биспидиновых молекул разной структуры на лизированных клетках печени крыс, где все соединения показали себя мощными активаторами процесса окисления полиаминов. Следующий этап исследования включал эксперименты с живыми клетками, моделями опухоли печени человека. Были отобраны 3 соединения из 8, уничтожающие раковые клетки в виде моно-компонента. Далее учёные применили комбинацию синтетического компонента с полиамином в нетоксических концентрациях. Как и ожидалось, эта комбинация оказалась смертельной для клеток опухоли и при этом не повредила здоровые клетки. Метод проточной цитометрии выявил, что гибель раковых клеток произошла именно в результате апоптоза.
Сами по себе полиамины, добавленные извне, не были токсичны ни для опухолевых, ни для нормальных клеток. Однако в присутствии биспидинов проявился противоположный эффект, а именно резкое снижение жизнеспособности опухолевых клеток. Исследователи объясняют это способностью биспидинов активировать функции энзимов — молекул, которые отвечают в организме за расщепление полиаминов и сопутствующий этому процессу выброс активных форм кислорода, который токсичен для опухолевых клеток. В раковых опухолях активность именно этого звена, участвующего в контроле за расщеплением полиаминов, нарушена, и токсичные для нездоровых клеток формы кислорода не образуются. Добавление биспидинов активирует путь метаболизма полиаминов и порождает токсичные для раковых клеток формы кислорода.
«Известен подход с введением в опухоль комбинации внешнего очищенного фермента с полиаминами. Мы же хотели восстановить собственную внутриклеточную активность ферментов распада полиаминов с помощью низкомолекулярных активаторов», — пояснил Дмитрий Жданов, доктор биологических наук, заведующий лабораторией медицинской биотехнологии института биомедицинской химии имени В.Н. Ореховича.
Исследование учёных Института биомедицинской химии имени В.Н. Ореховича и РУДН получило финансовую поддержку Минобрнауки России, результаты опубликованы в одном из научных журналов.
