Учёные вырастили электронные компоненты внутри мозга живых мышей
Учёные из Университета Пердью (Purdue University) предложили радикально новый подход к нейроинтерфейсам: вместо имплантации готовых электродов они формируют проводящие структуры прямо внутри мозга с помощью биохимических реакций. В основе метода — идея «выращивания» мягкой электродной сети, без классических жёстких имплантов.
Технология работает как локальная биофабрика. После инъекции химического прекурсора в мозговую ткань белки крови, включая гемоглобин, запускают реакцию, в результате которой формируется мягкая и гибкая проводящая сеть вокруг нейронов. Эта структура буквально повторяет форму ткани и движется вместе с ней.
Ключевое отличие нового подхода — возможность внешнего управления активностью мозга с помощью ближнего инфракрасного света. Световые импульсы воздействуют на сформированную сеть и могут временно подавлять активность нейронов, фактически «настраивая» работу отдельных участков мозга без прямого электрического раздражения.
Автор работы Кришна Джаянт (Krishna Jayant) отмечает, что «цель технологии — создать интерфейсы, которые выращиваются внутри мозга из собственных биохимических ресурсов организма и могут управляться извне без проводов и грубой хирургии».
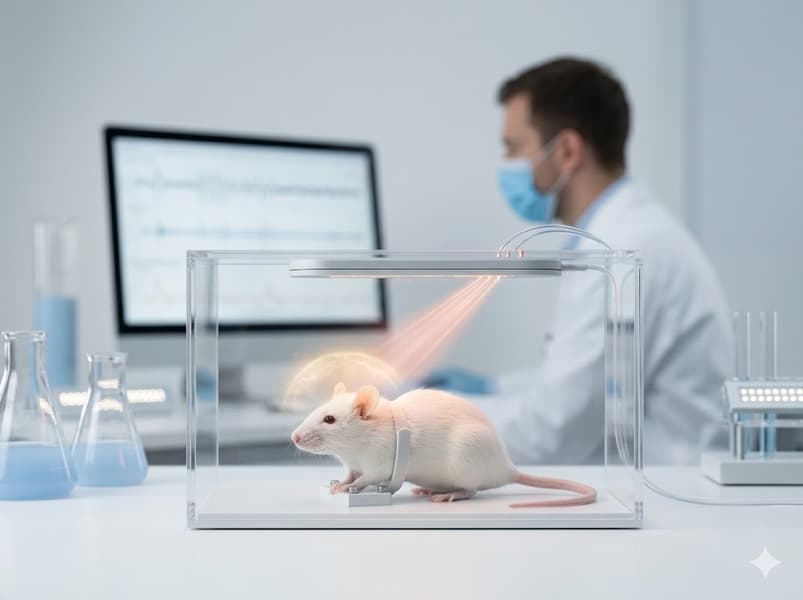 Иллюстрация: Nano Banana
Иллюстрация: Nano BananaСовременные нейроимпланты уже используются для восстановления речи и движения у пациентов с параличом, а также для терапии тяжёлых форм депрессии. Однако они основаны на жёстких микрочипах, которые требуют сложных операций и могут повреждать мягкие ткани мозга, вызывая воспаление, рубцевание и деградацию сигнала.
Именно несовместимость между «жёсткой электроникой» и «мягким мозгом» остаётся одной из ключевых проблем нейроинженерии. Даже при успешной установке такие устройства со временем теряют эффективность или требуют замены, что увеличивает риски при повторных операциях.
Новый подход относится к набирающему популярность направлению мягкой биоэлектроники. Ранее в этой области уже появлялись экспериментальные решения: например, шёлкоподобные сети, покрывающие поверхность мозга, или микроустройства, способные проникать в ткань с помощью иммунных клеток. Однако большинство таких систем остаются внешними или предварительно изготовленными структурами.
В отдельных исследованиях уже предпринимались попытки «собирать» проводящие материалы внутри живых тканей, но сталкивались с ограничениями: использовались токсичные катализаторы или системы, которые могли только считывать сигналы, но не влиять на них. Команда Пердью предложила альтернативу: использовать естественную биохимию организма как катализатор. По словам соавтора исследования Санкета Самала (Sanket Samal), «ключевая идея заключается в том, чтобы позволить телу самому выполнять сложную химическую работу».
Эксперименты показали, что реакция формирования проводящей структуры работает не только в живой ткани, но и в модельных системах. Например, введение материала в образцы приводило к формированию сети при температуре тела в течение суток. В экспериментах на эмбрионах рыбок данио (zebrafish) большинство организмов выжили и развивались нормально, что указывает на низкую острую токсичность.
На следующем этапе метод был протестирован на мышах. После минимально инвазивной инъекции в моторную кору мозга формировалась проводящая сеть, которая интегрировалась с нейронной активностью без признаков воспаления или перегрева.
Особый интерес вызвали эксперименты с дендритами — ветвящимися структурами нейронов, которые участвуют в обработке информации. В данном случае они сами участвовали в формировании проводящей сети, что позволило напрямую влиять на локальную нейронную активность.
Под действием ближнего инфракрасного света активность этих участков временно снижалась. У мышей это приводило к трудностям выполнения ранее выученного действия (нажатие рычага), однако после отключения света функция восстанавливалась, что говорит о обратимости эффекта и сохранности памяти.
Важным результатом стало отсутствие признаков инфекции, перегрева или выраженной иммунной реакции на протяжении серии экспериментов. Это особенно критично для любых технологий, работающих внутри центральной нервной системы.
Потенциальные применения включают лечение заболеваний, связанных с гиперактивностью нейронных сетей, таких как эпилепсия и болезнь Паркинсона, где сейчас используются либо медикаменты, либо инвазивные стимуляторы мозга. Однако учёные подчёркивают, что технология пока что на ранней стадии. Неизвестно, как долго такие структуры могут сохраняться в организме и насколько они безопасны при длительном использовании.
В перспективе метод может быть расширен за пределы мозга — например, для управления сигналами в спинном мозге или в сердечной ткани. Также обсуждается возможность добавления других функциональных материалов, включая магнитные компоненты для расширенного контроля активности. Конечная цель — создать интерфейсы, которые не просто взаимодействуют с мозгом, а становятся его частью, сохраняя стабильность на протяжении длительного времени.
iXBT прочитано 1521 раз