Cуперконденсатор объёмом 0,001 мм³ выдаёт напряжение 1,6 В, используя человеческую кровь как электролит
Рис. 1. Активные компоненты суперконеденсатора: электролит из кровотока, полимерные слои, золотые токосъёмники, электроды из биосовместимой смеси иономеров PEDOT: PSS, протонный сепаратор из поливинилового спирта (PVA), негативный фоторезист SU8
Физики из Хемницкого технического университета (Германия) и Дрезденского института по исследованию твёрдого тела и материалов (Leibniz IFW, Германия) разработали самый маленький в мире наносуперконденсатор, предназначенный для имплантации в человеческое тело.
Суперконденсатор не только безопасен для организма, но и использует кровь как электролит. Такой хитроумный трюк значительно уменьшает размеры устройства.
Изобретение относится к классу биологических наносуперконденсаторов (nBSC), которые не отличаются от обычных, кроме миниатюрных размеров и безопасной работы в человеческом теле для питания датчиков и имплантатов, вживлённых в организм.
Рис. 2. (а? d) Фотографии микроконденсатора до свёртывания в трубку «швейцарского рулета», шкалы 200 и 500 мкм. (f? j) Электрические характеристики устройства с различными электролитами: солевой физраствор, плазма крови, кровь
До настоящего времени размер лучших биосуперконденсаторов превышал 3 мм3 (1, 2, 3, 4, 5). Немецким физикам удалось сделать существенный шаг вперёд, уменьшив габариты примерно в 3000 раз.
На рисунке вверху — конструкция nBSC. Все слои помещаются на поверхность пластины, которая подвергается механическому напряжению, в результате чего слои отделяются и свёртываются в «рулет», формируя nBSC размером с пылинку.
Биосуперконденсатор особенно эффективен при использовании в крови, где он сохраняет до 70% ёмкости после 16 часов работы. Кроме того, устройство использует характерные окислительно-восстановительные ферментативные реакции в крови и живые клетки для подзарядки, что повышает его производительность на 40% (см. график саморазряда на рис. 3).
Устройство также хорошо выдержало нагрузки в аэродинамической трубе. Там симулировали условия кровеносных сосудов с изменением скорости потока и давления.
В ходе экспериментов удалось успешно использовать три устройства для питания крошечного датчика кислотности (рис. 5), который можно внедрить в кровеносные сосуды для регистрации отклонений pH, что указывает на рост опухоли и другие недуги.

Рис. 3. (а? с) Схематическая иллюстрация переноса ионов и накопления энергии между двумя рабочими электродами в различных электролитах. (d) Схематическая иллюстрация трёхэлектродной установки с рабочим электродом (измеряемый образец), электродом для сравнения (Ag/AgCl) и противоэлектродом (платиновый стержень) для определения окислительно-восстановительных/каталитических реакций
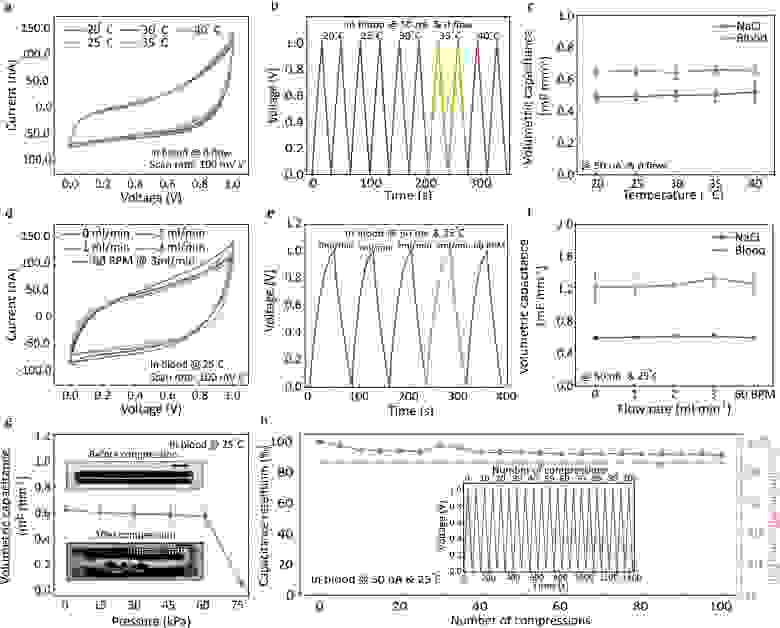
Рис. 4. Измерения в статическом потоке на разных температурах 
Рис. 5. Конструкция датчика кислотности крови, масштаб 200 мкм; изменение характеристик в зависимости от pH электролита
Научная статья опубликована 23 августа 2021 года в журнале Nature Communications (doi:10.1038/s41467–021–24863–6), в открытом доступе. Среди соавторов работы — Даниил Карнаушенко, Михаил Цуркан и Дмитрий Карнаушенко, все представляют Leibniz IFW.


