[Перевод] Обезболивающие, способные остановить кризис опиоидов

Каждый раз, когда Джеймс Задина [James Zadina] публикует новую работу или упоминание в прессе, телефон в его лаборатории в Новом Орлеане начинает звонить. Электронные письма переполняют ящик. От людей со всей страны приходят сообщения с жалобами на боль.
«Мне звонят и говорят, «У меня такие ужасные боли. Когда появится ваше лекарство?»,- говорит Задина. А я отвечаю «Не могу вам сейчас его дать, работаю так быстро, как только могу». Это всё, что я могу сказать. Но это сложно».
Последние 20 лет Задина, исследователь в Медицинской школе Тулейнского университета и Системе здравоохранения ветеранов Юго-восточной Луизианы, находится на переднем краю битвы с древним врагом человечества: физической болью. В последнее время его работа обрела новую срочность. В США смертность от опиоидов и привязанности к ним достигает масштабов эпидемии и Задина пытается создать новый вид обезболивающих препаратов, не обладающий такими разрушительными побочными эффектами, какие оказывают часто выписываемые препараты вроде Оксикодона.
Его поиски осложнены тем, что те же самые механизмы, которые позволяют лекарствам эффективно нейтрализовывать боль, отвечают и за привыкание, и за злоупотребление лекарством. Так же, как их близкий химический кузен героин, опиоиды могут вызвать у людей физическую зависимость. Исследователи десятилетиями пытались «разделить свойства, способствующие привыканию к опиатам и болеутоляющие свойства», говорит Дэвид Томас, администратор в Государственном институте наркотической зависимости и один из основателей Консорциума по вопросам боли в Государственном институте здоровья. «Они идут рука об руку».
Но Задина считает, что уже близок к их разделению. Буквально прошлой зимой он со своей командой опубликовал работу в журнале Neuropharmacology, в которой описывал, как они избавили крыс от боли без появления у тех пяти самых распространённых побочных эффектов, связанных с опиоидами, включая увеличенную переносимость, нарушение двигательных функций, подавление дыхания, что является причиной большинства связанных с опиоидами смертей. Следующий шаг — тестирование на людях.
Это лишь одна из многих попыток покончить с долговременным уроном, наносимым во время избавления людей от боли. По информации Государственного института наркотической зависимости, до 8% пациентов, которым прописали наркотические болеутоляющие для хронических болей, вырабатывают зависимость. Поэтому пациентам было достаточно сложно доставать такие опиоиды, как кодеин, для уменьшения болей, говорит Томас. Эта ситуация начала меняться в 1990-х. Новые опиоиды, например, Оксикодон (и новые рекламные кампании фармацевтических компаний) сошлись с убедительными требованиями докторов, лечащих боль и защитников пациентов, утверждавших, что многие люди с хроническими болями –, а от этого недуга страдают примерно 100 миллионов американцев — мучаются без необходимости.
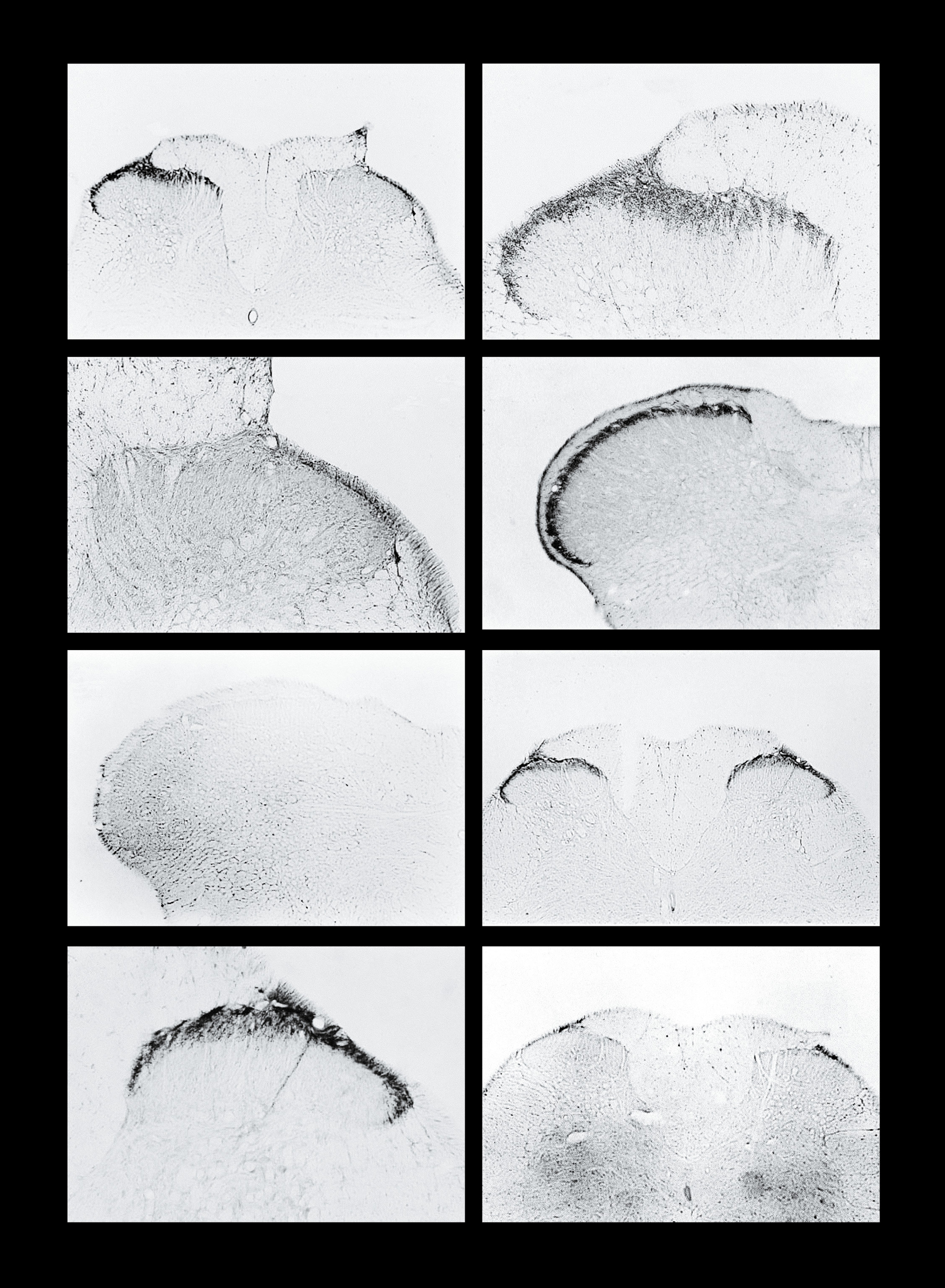
Болеутоляющая субстанция, эндоморфин, реагирует с клетками спинного мозга крыс
Но маятник качнулся обратно так далеко, что опиоиды стали лекарством по умолчанию, даже при наличии лучших альтернатив. Дэн Клаув [Dan Clauw], директор Исследовательского центра утомления и хронических болей при Мичиганском университете, говорит, что слишком много докторов сообщают пациентам «Меня учили, что опиоиды хорошо справятся с любым типом боли и если боль слишком сильная, а вы уже отчаялись, я попробую это лекарства, несмотря на риск привыкания».
Последствия оказались разрушительными. В 2014 году количество смертей от передозировки опиоидов превысило 18 000, примерно 50 человек в день — в три раза больше, чем было в 2001 году. И эта статистика ещё не включает пациентов, перешедших на героин, чтобы удовлетворить свою тягу. Чиновники из Центров контроля над распространением заболеваний сравнили эту проблему с эпидемией ВИЧ в 1980-х.
Разработка болеутоляющих лучшего качества сталкивается с трудностями, поскольку боль в нашем теле идёт по сложным путям. Достигающие мозга сигналы, интерпретируемые, как боль, иногда возникают из-за проблем на периферии, или на поверхности тела, как в случае порезов. В других случаях источник боли лежит глубже: он происходит от повреждения нервов, случающегося от серьёзной раны или травмы спины. Исследователи, в частности, Клаув, находят доказательства того, что многие болевые синдромы обусловлены третьим типом боли: сбоями в работе мозга.
Но наличие таких разных механизмов возникновения боли означает, что существует несколько разных способов решения проблемы опиоидов. Пока Задина и другие учёные пытаются устранить опасные свойства опиоидов, другие обезболивающие могут быть нацелены на принципиально другие механизмы тела.
Основной способ справиться с болью — уменьшить сигналы, отправляемые телом в мозг.
Почти во всех наших тканях есть т.н. «ноцицептивные» нервные окончания, крохотные волокна, собирающие информацию и передающие её в центральную нервную систему и на обработку в мозг. Эти волокна работают болевыми датчиками. Некоторые нервные окончания реагируют на давление, отправляя электрические импульсы в спинной мозг, и тогда мы чувствуем боль. Другие окончания реагируют на изменение температуры, создавая сигналы боли, если нам слишком холодно или слишком жарко. После получения травмы к этому месту прибывают воспалительные клетки и выпускают десяток различных химических веществ, которые вызывают другие клетки для борьбы с патогенами, расчистки обломков и начала строительства новых клеток. Но эти же воспалительные клетки приводят к тому, что нервные окончания на месте травмы отправляют больше болевых сигналов. При локальном повреждении, например, когда вы потянули лодыжку или вывихнули колено, лёд или противовоспалительные средства вроде ибупрофена, могут заглушить болевые сигналы.
Но иногда, после тяжёлой травмы, ампутации, диабетического повреждения нервов, нервные волокна или клетки, из которых они происходят, физически изменяются. В них могут включаться или выключаться некоторые гены. Это меняет количество или тип активных клеточных машин, известных как натриевые каналы — протеинов, торчащих из клеток и регулирующих их возможность генерации электрических импульсов. Нервные клетки могут общаться друг с другом посредством этих импульсов и внезапная активность дополнительных натриевых каналов может привести к тому, что нерв будет выдавать импульсы, как пулемёт, «спонтанно, даже в отсутствие угрожающих стимулов», поясняет Стивен Ваксман [Stephen Waxman], профессор нейрологии в Йельском университете, управляющий Центром исследования нейрологии и регенерации в Госпитале по делам ветеранов в Коннектикуте. Эти импульсы причиняют людям острую боль. Одна из распространённых причин — химиотерапия. «Иногда боли такие сильные, что люди говорят «Я не могу её терпеть», говорит Ваксман. «Я лучше умру от рака, чем буду испытывать боли от лечения».
Есть девять типов натриевых каналов. Обезболивающее, используемое дантистами, способно локально притупить все сразу. Но такой подход не сработает в общем случае, поскольку некоторые из этих каналов присутствуют в мозгу и центральной нервной системе. Но Ваксман входит в костяк исследователей, ищущих способы воздействия только на один ключевой канал. Он открыл его важность, изучая людей с генетическими отклонениями, препятствующими формированию этого канала. В их теле отсутствует этот канал, и они живут, не чувствуя боли. И наоборот, люди, родившиеся с гиперактивным вариантом этого канала, чувствуют, «будто их тело соприкасается с лавой», говорит Ваксман.
Лекарство, создаваемое на основании открытий Ваксмана компанией Pfizer, протестировано на пяти пациентах. Кроме того, уже разрабатываются аналогичные обезболивающие. Теоретически, у них не должно быть серьёзных побочных эффектов.
Что и возвращает нас обратно к опиоидам.
Наши периферические нервы, отправляющие нам сигналы боли, идут к позвоночному столбу, где соединяются с нервными клетками, переносящими сообщения в центральную нервную систему и к нейронам в мозге, после чего мы и начинаем чувствовать боль.
Именно тут все опиоиды, от Оксикодона до героина и морфина, творят своё волшебство. Делают они это, привязываясь к мю-рецепторам на стыках, где встречаются нервные клетки. Это приводит к щелчку переключателя, уменьшающего возможность этих клеток выдавать сигналы. И когда нервные волокна на периферии тела отправляют сигналы боли в мозг, нейроны, которые заставляли бы нас чувствовать боль, не отвечают.
«Опиоиды не затрагивают источник боли, они лишь отключают осознание боли мозгом»,- говорит Льюис Нельсон [Lewis Nelson], профессор скорой помощи в Медицинской школе Нью-Йоркского университета, заседавший в комиссии, выпустившей рекомендации по использованию опиоидов в Центрах по борьбе с заболеваниями. «Небольшая доза опиоида изменяет ощущение от чрезвычайно раздражающего, до такого, о котором можно не задумываться».
Мю-рецепторы реагируют не только на обезболивающие, но и на «эндогенные опиоиды» — естественные сигнальные соединения, производимые нашим телом, типа эндорфинов, вырабатывающихся при упражнениях и приводящих к «кайфу бегуна». Проблема в том, что тело не реагирует на лекарства вроде героина или Оксикодона так же, как на эндогенные вещества.
В отличие от эндогенных опиоидов, обезболивающие лекарства часто активируют особые клетки в ЦНС, известные, как глия. Глия подчищают клеточные обломки в теле и помогают управлять реакцией на травмы центральной нервной системы. После активации они производят воспалительные вещества, которые могут привести к тому, что тело зарегистрирует больше болевых сигналов. Многие исследователи верят, что увеличение активации глиальных клеток может приводить к привыканию, из-за чего опиоиды со временем теряют эффективность и пациенту требуются увеличенные дозы для достижения эффекта. В конце концов эти дозы могут привести к смертельно опасным проблемам с дыханием.
Всего этого можно было бы избежать, если бы Задина смог разработать синтетический опиоид, больше похожий на собственные вещества тела — такие, которые воздействуют на мю-рецепторы, не затрагивая глиальные клетки. В 1990-х он с командой изолировал ранее неизвестное нейрохимическое соединение в мозгу, вещество, уменьшающее боль, которое назвали эндоморфин. С тех пор он пытается создать его улучшенную синтетическую версию.
И одной из версий было лекарство, проверенной Задиной на крысах, что было описано в работе, опубликованной прошлой зимой в журнале Neuropharmacology. Как и в случае с другими соединениями, разработанными им, эта версия показала себя не хуже, а может и лучше морфина в деле избавления животных от боли без возникновения побочных эффектов. Теперь он ведёт переговоры с несколькими инвесторами и биотехнологическими компаниями, интересующимися в превращении этого вещества в лекарство. Когда он с коллегами найдёт достаточно денег для открытия свой компании, или подпишет договор с партнёром по лицензии, они будут запрашивать одобрения на проведение ранних тестов на людях. «Пока не проверишь на людях, не узнаешь»,- говорит он.
Лекарство Задины всё равно, скорее всего, будет активировать области мозга, связанные с вознаграждением и может приводить к лёгкой эйфории, что может склонить кого-то к зависимости. Но быстрое привыкание, обычно происходящее с опиоидами — и симптомы ломки, сопровождающие людей, прекращающих принятие лекарств — скорее всего, исчезнут. «Я хочу устранить дилемму, встающую перед врачами и пациентами, «Устранить ли боль полностью с риском вызвать зависимость, или устранить её не полностью, потому что я не хочу использовать опиоиды?- говорит Задина. — Это мой главный стимул».
Но даже в случае успеха этого нового лекарства, ни он, ни новые обезболивающие, работающие с натриевыми каналами, не смогут справиться с новым типом боли, о существовании которого мы до недавнего времени не подозревали — боли, которая не реагирует на опиоиды. Клаув из Мичигана изучает эту разновидность боли последние 20 лет. Исходя из снимков мозга, он определил, что она происходит из-за неправильной работы нейронов, а не из-за проблемы в том месте, которое кажется источником боли. Он считает, что это самая распространённая причина боли в молодых людях, страдающих от заболеваний, ставивших докторов в тупик, включая фибромиалгию, определённые головные боли и синдром раздражённого кишечника. Что должны принимать эти пациенты вместо часто прописываемых им опиоидов? Многие, по словам Клаува, должны принимать лекарства, устраняющие неправильную активацию нейронов путём усиления нейротрансмиттеров. Некоторые лекарства, разрабатывавшиеся как антидепрессанты, способны достигать такого эффекта.
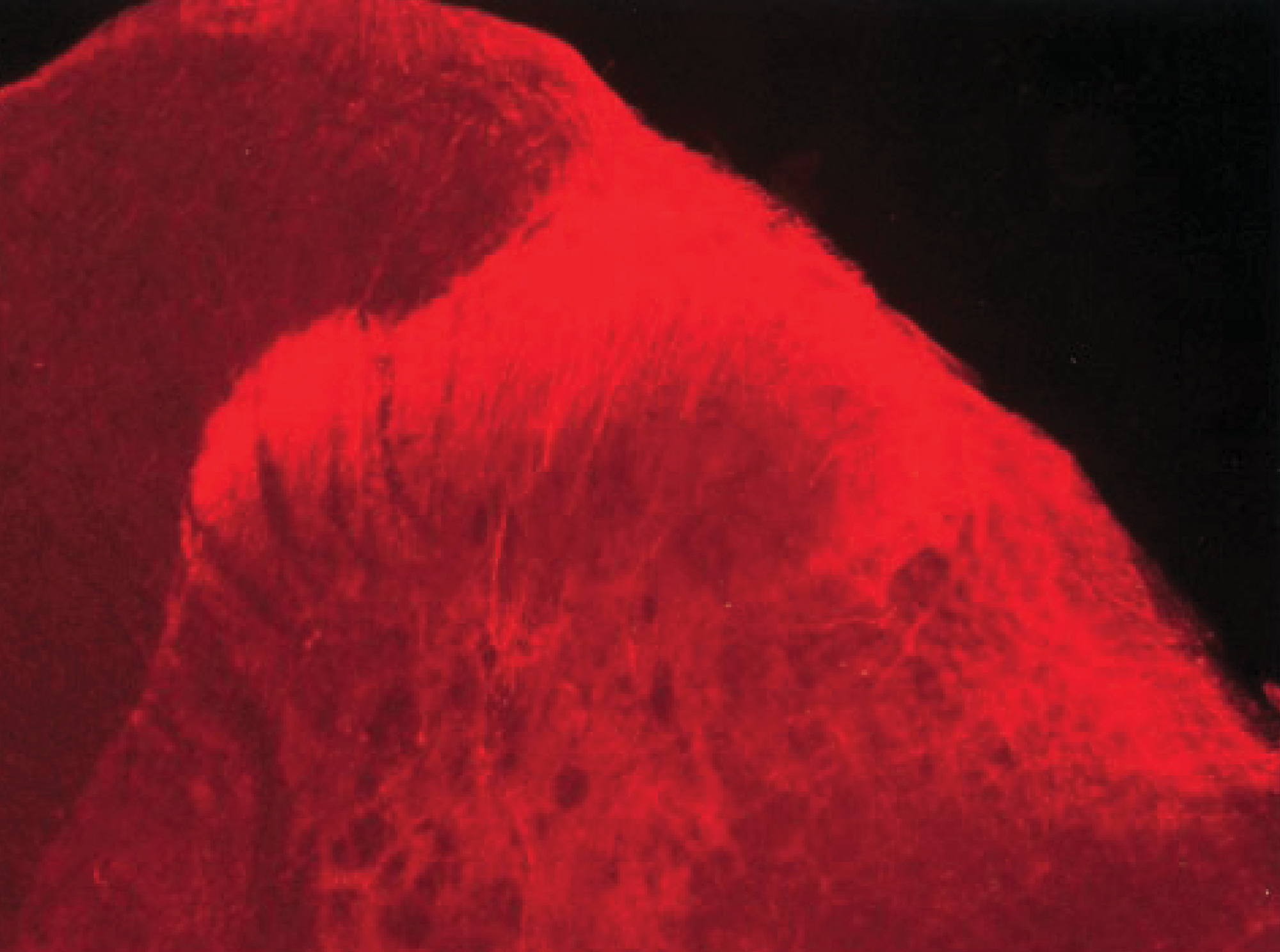
Изображение из работы 1998 года, доказывающее присутствие эндоморфина в путях, по которым боль передаётся в мозг
Томас из Государственного института здоровья считает, что исследование Клаува доказывает, что опиоиды сегодня прописывают чрезмерно часто.
«Если вы попали в ДТП, пострадали в бою, у вас оторвало руку, или что-то подобное, и вам действительно очень больно, они отрубят сильные боле очень быстро,- говорит Томас. — Но сейчас их используют во множестве разных случаев, когда опиоиды не пойдут пациенту на пользу в долгосрочной перспективе».
